|
Aguas
duras:
una cuestión de iones |
|
![]() |
|
 Prácticamente
en todos los sectores de producción industrial
se utiliza agua, pero ninguno
de ellos está exento de los efectos de
sus componentes naturales. Una
de las clases de impureza, y la que mayor atención
se lleva, es la dureza del agua. Prácticamente
en todos los sectores de producción industrial
se utiliza agua, pero ninguno
de ellos está exento de los efectos de
sus componentes naturales. Una
de las clases de impureza, y la que mayor atención
se lleva, es la dureza del agua.
Nos referimos a la presencia
de iones disueltos (partículas sólidas
con carga eléctrica neta), en especial
iones de calcio [Ca2+]
y iones de magnesio [Mg2+]
cuyas cargas netas son positivas (cationes), y
que provienen de la erosión y desintegración
de rocas calcáreas y sedimentos varios
presentes en el medio ambiente, principalmente
en aguas subterráneas.
La carga positiva de estos
cationes sólidos se balancea con la presencia
de aniones (con carga neta negativa),
de los cuales los más influyentes son los
bicarbonatos [HCO3-
] y los carbonatos [CO32-].
Estos aniones tienen su origen en el dióxido
de carbono [CO2] disuelto naturalmente
en el agua.
Los iones con cargas netas
opuestas intervienen en un buen número
de fenómenos químicos, entre ellos
la cristalización (origen
de las incrustaciones calcáreas) y reacciones
electroquímicas de oxidación
(origen de la corrosión galvánica).
Ambos procesos ocurren de forma
espontánea siempre que participen
en el sistema compuestos salinos,
agua, oxígeno
disuelto, un medio ácido,
y la superficie metálica propensa a recibir
las incrustaciones y a corroerse.
 Más acerca de Corrosión natural
Más acerca de Corrosión natural |
|
Cristalización: origen de
las incrustaciones |
|
![]() |
|
 Los iones de signo opuesto se unen entre sí
(debido a fuerzas electrostáticas naturales)
mediante enlaces iónicos siguiendo
un esquema regular y ordenado que se manifiesta
bajo la forma de un cristal,
siendo éstos los responsables del aspecto
sólido y consistente de las sales. El enlace
iónico se funda en la fuerza de
atracción electrostática entre iones
de cargas netas opuestas (aniones
y cationes).
Los iones de signo opuesto se unen entre sí
(debido a fuerzas electrostáticas naturales)
mediante enlaces iónicos siguiendo
un esquema regular y ordenado que se manifiesta
bajo la forma de un cristal,
siendo éstos los responsables del aspecto
sólido y consistente de las sales. El enlace
iónico se funda en la fuerza de
atracción electrostática entre iones
de cargas netas opuestas (aniones
y cationes).
La cristalización
ocurre bajo condiciones muy comunes en muchos
campos de aplicación:
1. Sobresaturación
de iones sólidos en solución (mayor
cantidad de lo que la solución admite en
estado de equilibrio)
2. Nucleación
inicial de cristales debido a la combinación
de iones de la solución con iones
no pertenecientes a la fase líquida,
(i.e. superficies metálicas en contacto
con la fase líquida)
3. Crecimiento
de cristales por propio enlace iónico con
otras sales precipitadas.
4. Otros
factores como incrementos bruscos de
temperatura, turbulencia en el sistema, naturaleza
y estado de la superficie en contacto con la solución
y presencia de otras impurezas. |
|
Formas de cristalización: Calcita y Aragonita |
|
![]() |
|
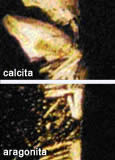 La
cristalización de iones en solución,
bajo las condiciones mencionadas produce la formación
de compuestos iónicos,
como sales de calcio y de magnesio,
de gran dureza y con fuerte capacidad de adherencia
a las superficies de tuberías, circuitos
y en especial, a zonas de trasferencia de calor. La
cristalización de iones en solución,
bajo las condiciones mencionadas produce la formación
de compuestos iónicos,
como sales de calcio y de magnesio,
de gran dureza y con fuerte capacidad de adherencia
a las superficies de tuberías, circuitos
y en especial, a zonas de trasferencia de calor.
Las incrustaciones están
compuestas fundamentalmente por calcita
en mayor proporción, y por aragonita
en menor proporción. Ambos son carbonatos
de calcio con igual composición
química, aunque distina estructura
cristalina, físicamente hablando.
La calcita tiene una capacidad incrustante
holgadamente superior frente
a la aragonita. Esto será de fundamental
importancia para comprender el efecto
desincrustante del Equipo Magnético
Permanente IONIS.
|
|
Incrustaciones:
nuestro eje central de atención |
|
![]() |
|
 De
no aplicarse un efectivo control de estas reacciones
naturales, la adhesión constante
y progresiva de carbonatos
de calcio y de magnesio provoca el crecimiento
de una costra incrustante
de muy importantes espesores, la cual es mecánicamente
dura de remover y térmicamente
muy aislante, lo cual reduce espectacularmente
la eficiencia de la transferencia
de calor al agua (i.e. calderas). De
no aplicarse un efectivo control de estas reacciones
naturales, la adhesión constante
y progresiva de carbonatos
de calcio y de magnesio provoca el crecimiento
de una costra incrustante
de muy importantes espesores, la cual es mecánicamente
dura de remover y térmicamente
muy aislante, lo cual reduce espectacularmente
la eficiencia de la transferencia
de calor al agua (i.e. calderas).
 Más
acerca de Pérdida de eficiencia térmica Más
acerca de Pérdida de eficiencia térmica
Esto no sólo implica
pérdida de capacidad de
caudal en tuberías, sino también
excesos de consumo de energía
para producir calentamiento o enfriamiento, y
más importante aún, el incremento
de posibilidades de fallas catastróficas
en maquinarias sobrecalentadas.
 Más
acerca de Factores estratégicos clave Más
acerca de Factores estratégicos clave
|
